ユアンフェンPOV: EUDAMEDのタイムラインを更新
EU委員会は最近,EUDAMEDの完成と実施に関する更新を2024/1860修正に基づいて発表しましたこの記事では,EUDAMEDの現在のスケジュールと,これらのスケジュールに対する我々の見解を概説し,業界がそれに応じて準備するのを助ける..
現在のEUDAMEDのスケジュール:
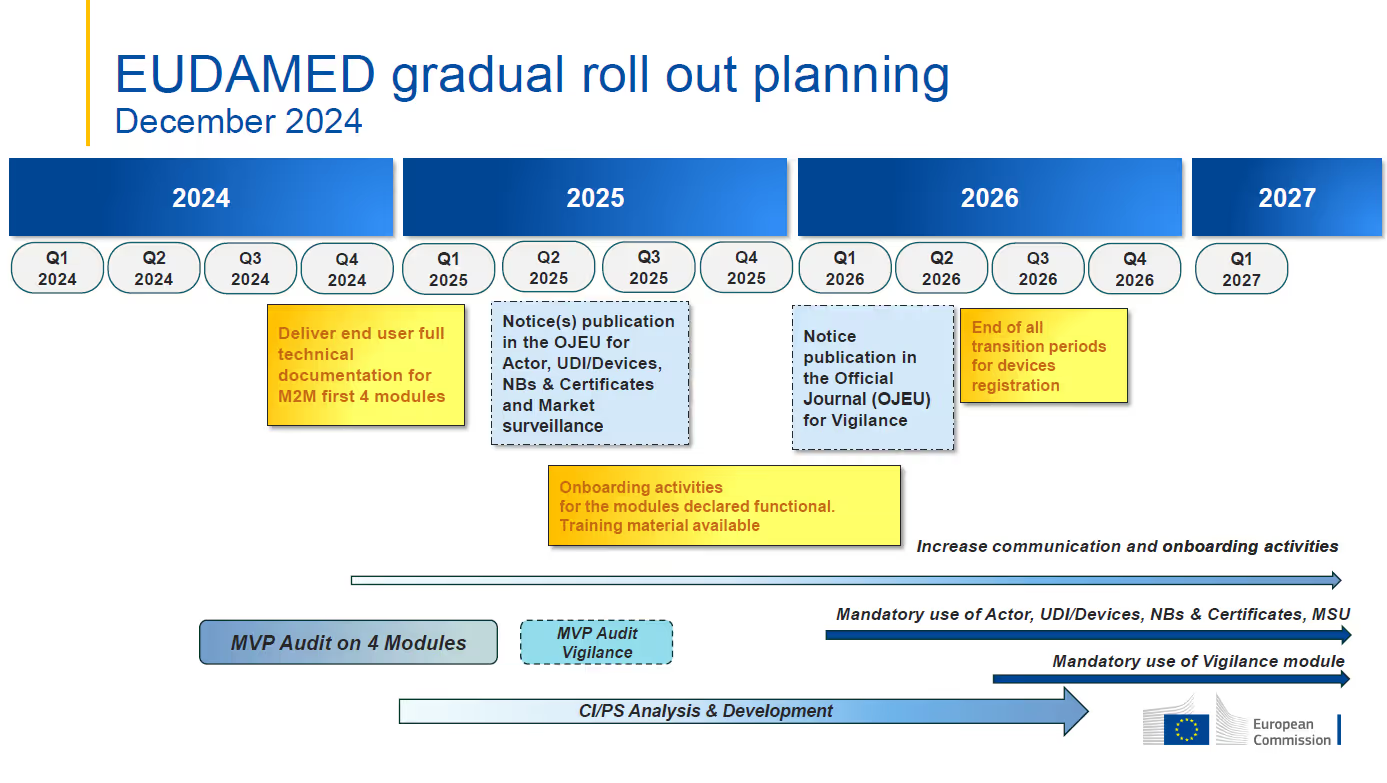
- 機能的なEUDAMEDモジュールの最初の強制的な適用の目標日は2026年1月1日です.監視モジュールは2026年第3四半期から義務化され,EUDAMEDの完全な機能は2027年第2四半期に予定されています..
- 現在,Actor,UDI&Devices,証明書,市場監視のモジュールが監査されています.独立した最小可活性製品 (MVP) 監査は,監査準備ができていると認められたモジュールの機能と相互接続性を評価し確認することを目的としています.この監査は2025年第2四半期までに完了する予定です
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)アクター,UDI&デバイス,証明書,市場監視モジュールは2025年第2四半期の終わりに完全に機能するよう宣言され,1月1日の強制的な適用日が決定される予定です. 2026.
わかった - 2025年第2四半期の終わりまでにActor,UDI&Devices,証明書,市場監視モジュールが完全に機能し,2026年1月1日に産業使用が義務付けられる予定です.
- 警戒モジュールは MVP 監査の一環ではなく,上記モジュールと共に完全に機能していないと宣言されます.改訂された時間軸は,そのモジュールの監査が2025年第2四半期から第3四半期の間に行われることを示しています2026年第2四半期に 強制的な申請を予定しています
わかった - 臨床試験/パフォーマンス研究 (CI/PS) モジュールの開発は2026年第3四半期まで継続する予定です.CI/PS モジュールを評価するための監査は,他の5つのモジュールと共に,CI/PS MVPが開発された後に完了します..
わかった
フォト キュリティー欧州委員会
EUDAMEDの完成と実施のための更新を発表しました.修正案2024/1860この記事では,EUDAMEDの現在のスケジュールと,これらのスケジュールに対する我々の見解を概要し,業界がそれに応じて準備するのを支援します.
現在のEUDAMEDのスケジュール:
- 機能的なEUDAMEDモジュールの最初の強制的な適用の目標日は2026年1月1日です.監視モジュールは2026年第3四半期から義務化され,EUDAMEDの完全な機能は2027年第2四半期に予定されています..
- 現在,Actor,UDI&Devices,証明書,市場監視のモジュールが監査されています.独立した最小可活性製品 (MVP) 監査は,監査準備ができていると認められたモジュールの機能と相互接続性を評価し確認することを目的としています.この監査は2025年第2四半期までに完了する予定です
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)アクター,UDI&デバイス,証明書,市場監視モジュールは2025年第2四半期の終わりに完全に機能するよう宣言され,1月1日の強制的な適用日が決定される予定です. 2026.
わかった - 2025年第2四半期の終わりまでにActor,UDI&Devices,証明書,市場監視モジュールが完全に機能し,2026年1月1日に産業使用が義務付けられる予定です.
- 警戒モジュールは MVP 監査の一環ではなく,上記モジュールと共に完全に機能していないと宣言されます.改訂された時間軸は,そのモジュールの監査が2025年第2四半期から第3四半期の間に行われることを示しています2026年第2四半期に 強制的な申請を予定しています
わかった - 臨床試験/パフォーマンス研究 (CI/PS) モジュールの開発は2026年第3四半期まで継続する予定です.CI/PS モジュールを評価するための監査は,他の5つのモジュールと共に,CI/PS MVPが開発された後に完了します..
わかった

フォト キュリティー欧州委員会
Rimsys は,この発表が各利害関係者グループに与える影響を以下のように見ています.
ユアンフェン
UDIは 警戒モジュールとの 将来の相互作用と同様に 前提ですRimsysは,更新された目標日程に関係なく,UDIと市場監視後の機能の開発を継続する我々はまた,EUDAMEDと機械対機械 (M2M) 能力で相互作用するためのデータ転送 (DTX) 能力の確立の潜在的な影響を認識しています.EUDAMED に M2M DTX に必要な最終的な要件が公表されEUDAMEDソリューションの一部として M2M能力を提供します.
業界/顧客
欧州委員会はEUDAMEDの時間軸を複数回更新したため,業界が新しい目標日程を受け入れるのを躊躇すると予想しています.これはEUDAMEDの準備に再関与を遅らせる可能性がありますしかし,我々は,欧州委員会がこれらの更新された期限を推し進めるのを期待していない.EUDAMED に今年第2四半期までにデータを送信する計画がない製造者は,これらの期限を満たすには大きな課題が待ち受けている.期待されるモジュールの監査が進行中であり,関連する技術文書が公開されているため,Rimsysは,規制データを今から整理し,その情報を利用可能なEUDAMEDモジュールすべてに早期に提出するための措置をとることを推奨しています.
欧州委員会
ECは,業界に,その解決策を確立し,データを自発的に提出することを強く推奨しています.待ってはいけません.早期にデータを送信することで 企業がメリットを得ることができ,世界中のメディテック産業が攻撃する前に データが入手できるようになる.EUDAMED が義務化される.これらの企業は,データ提出の問題が発生した場合,委員会のリソースと協力するために,ラインの先端にもいます.
* 注記 - この記事には,規制の解釈とユアンフェンこの情報は,規制当局の公式のガイドラインを代替するものではありません.

